周其林、朱守非团队发展了炔基卡宾对Si-H键的不对称插入新反应,为手性炔丙基硅烷和联烯基硅烷的结构多样性合成提供了新的有效方法。相关成果发表于J. Am. Chem. Soc.(https://doi.org/10.1021/jacs.1c03435),论文第一作者为杨亮亮博士。
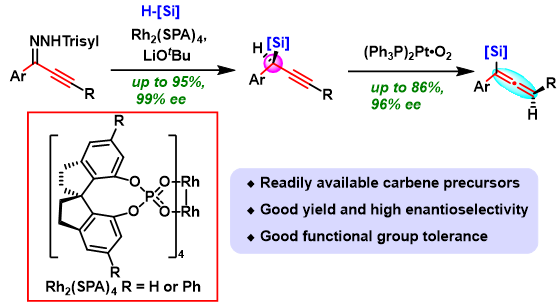
有机硅化合物广泛应用于有机合成、材料、医药等领域,其中手性炔丙基硅和手性联烯基硅因其可进行多种多样的转化,已经成为一种重要的手性砌块(图1A)。目前,手性炔丙基硅主要是从手性原料出发制备,不对称催化合成方法报道很少。近年来,手性联烯基硅化合物的合成受到广泛关注,取得了很大的进展,然而,大部分合成方法都是基于炔丙醇衍生物的取代反应。由于合成方法的限制,现有的手性炔丙基硅和手性联烯基硅的结构多样性较差,阻碍了它们的应用研究。
最近,南开大学化学学院周其林、朱守非团队利用他们此前发展的手性螺环磷酸双铑催化剂(J. Am. Chem. Soc. 2020, 142, 12394),实现了炔基卡宾对Si-H键高对映选择性插入反应,直接从简单易得的炔基磺酰腙合成光学活性的炔丙基硅烷(图1B)。这也是首例炔基卡宾的高对映选择性插入反应。手性炔丙基硅烷可以通过一种非均相铂催化剂,高度立体保持地异构化为轴手性联烯基硅烷。
研究者评价了一系列炔基磺酰腙底物。使用螺环磷酸双铑催化剂C1,炔基端位为芳基的底物都能够以较高的收率(64-92%)和对映选择性(78-96% ee)生成炔丙基硅烷(图1,Condition A)。含有噻吩基团的底物也能够给出很好的对映选择性。当底物的炔烃端位与烷基、烯基、炔基等相连时,5,5’-位苯基取代的螺环磷酸双铑催化剂C2能够给出最优的结果(图1,Condition B)。该反应能够兼容烯烃、炔烃、卤素、醚键、吲哚等多种官能团。

图1. 炔基磺酰腙和硅烷的不对称插入反应
根据以往文献中炔基磺酰腙参与的卡宾转移反应和卡宾对Si-H键的插入反应机理研究,研究者提出了该反应的催化循环。首先,炔基磺酰腙在碱作用下,生成活泼的炔基重氮甲烷。然后,催化剂分解重氮生成炔基铑卡宾物种Int-IV。最后,Int-IV物种对Si-H键进行插入生成目标产物(图2)。密度泛函理论计算表明,手性螺环磷酸配体在铑中心所构成的拥挤的手性口袋,使Si-H键更容易从re面进攻铑卡宾中间体,生成R构型的产物,这和实验结果相吻合。
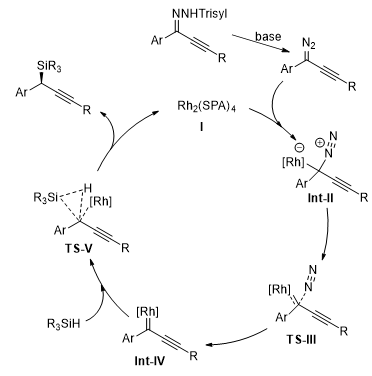
图2. 反应的催化循环
在克级规模实验中,催化剂用量可以降至0.15 mol%,反应依然能够取得较高的收率(75%)和优秀的对映选择性(94% ee)(图3A)。此外,通过氢化和硼氢化反应,手性炔丙基硅烷能够转化为多种手性烯丙基硅烷(图3B)。
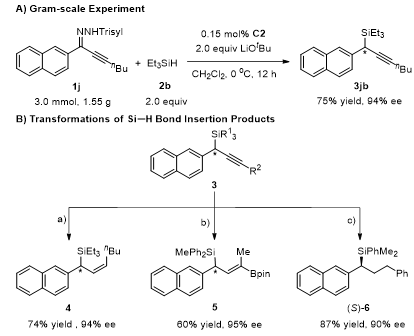
图3. 克级规模反应及产物转化
为了进一步展示炔基卡宾对Si-H键的不对称插入反应的潜在应用价值,研究者进一步研究了炔丙基硅烷异构化为联烯基硅烷的反应。他们发现(Ph3P)2Pt·O2能够催化炔丙基硅烷异构化为联烯基硅烷,且对映选择性能够得到很好的保持(图4)。该反应的活性催化物种可能是现场生成的纳米铂。他们培养了联烯基硅烷 (S)-7b的单晶,确定了产物的绝对构型。
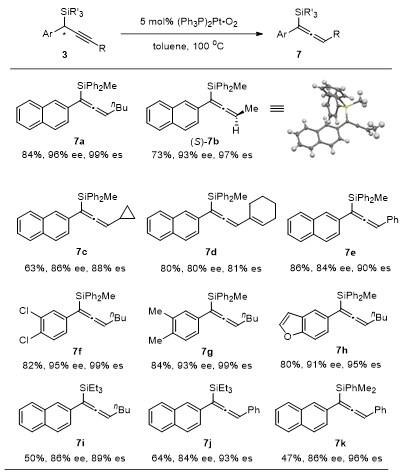
图4. 炔丙基硅烷的异构化反应(es = 产物的ee值/原料的ee值)
总之,上述研究首次实现了炔基卡宾对Si-H键高对映选择性插入反应,以简单易得的炔基磺酰腙作为原料,合成了多种新型手性炔丙基硅烷,并进而在铂催化下高度立体保持地异构化为手性联烯基硅烷。这些工作拓展了卡宾转移反应的类型,深化了对炔基取代卡宾反应性的认知,为手性有机硅的结构多样性合成提供了新的方法。




