来源:研之成理

▲第一作者: 王衍伟
通讯作者: 仇友爱
通讯单位: 南开大学
论文DOI:10.1002/anie.202210201
CO2作为储量丰富、廉价易得且可再生的C1资源,其催化转化生成高附加值的化学品一直是合成化学领域的研究热点。从绿色有机合成化学研究的角度来看,CO2在催化剂的作用下与简单有机化合物反应生成含有羧基单元的反应具有原子经济性高和经济实用的优势。近年来,过渡金属催化的碳−卤键与CO2偶联羧化反应受到了广泛地关注,该类反应通常需要加入当量的金属还原剂或者结合光催化来实现(图1A,上)。然而,在实际生产中,特别是药物合成化学中,对金属残留量的要求非常苛刻,痕量的金属在后处理过程中往往需要很高的成本。因此,发展绿色、高效的非金属催化的碳−卤键羧化方法是非常有必要的。
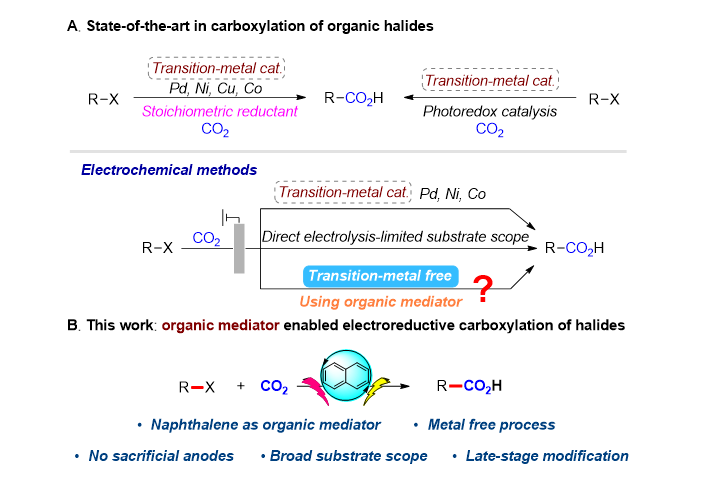
▲图1. 碳−卤键与CO2偶联羧化的反应
近些年来,有机电化学合成作为一种绿色高效的合成方法,得到了飞速的发展。电化学条件下可以通过调节电极电势选择性地实现官能团的氧化或者还原。然而由于碳卤键自身的高还原电势,通过电化学还原活化,往往因电势过高导致官能团兼容性差,导致底物范围非常窄。电化学结合过渡金属催化在一定程度上可以解决该问题,通过间接电解的模式,提高反应的选择性以及官能团容忍性,但是有机媒介促进的电化学碳−卤键羧化仍然鲜有报道。
近日,南开大学化学学院元素有机化学国家重点实验室仇友爱课题组在绿色有机电合成的前期工作基础上(Angew. Chem. Int. Ed. 2022, 61, e202115178.; Nat. Commun. 2022, 13, 3774.; Angew. Chem. Int. Ed. 2022, e202207746),报道了一类新型的有机还原媒介促进的碳−卤键电化学羧化反应。该反应使用催化量的萘作为电化学还原媒介;使用CO2作为羧基源;具有良好的底物适用范围;反应不需要牺牲阳极,反应条件温和简单,对后修饰的天然产物也表现出很好的兼容性(图1B)。
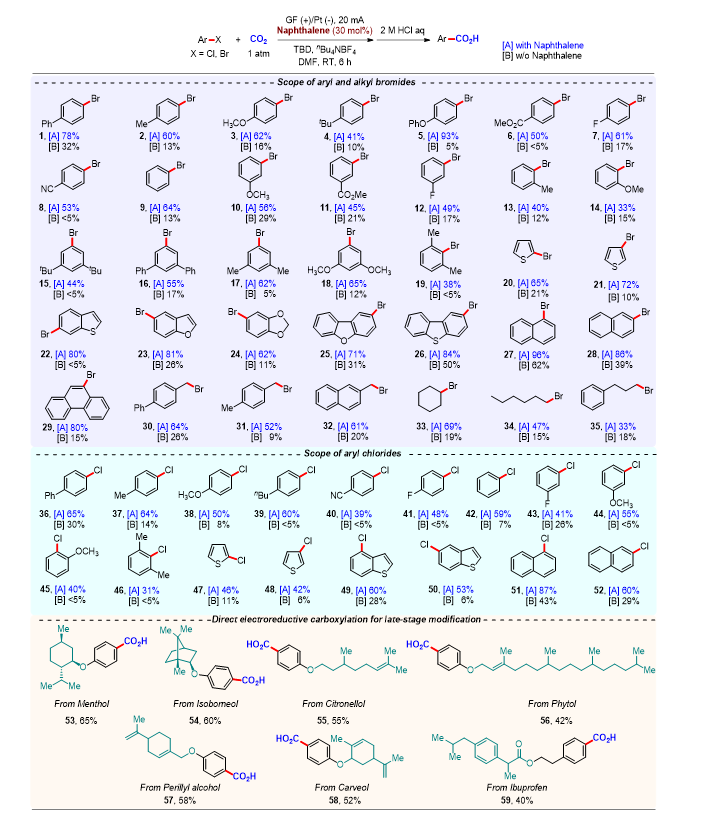
▲图2. 反应底物拓展
该方法的底物普适性好,适用于不同基团取代的芳基溴化物和芳基氯化物,以中等到优秀的收率生成相应的苯甲酸类化合物。对于具有较高还原电势的富电子芳基卤化物,反应也能够顺利进行。值得一提的是,该方法还可以适用于简单的烷基溴化物,以中等收率生成相应的简单烷基羧酸类化合物。控制实验表明,萘在该反应过程中起到了非常关键的作用;不添加萘媒介的时候,该反应主要生成脱卤氢化的产物。针对复杂的芳基溴化物,如药物活性分子薄荷醇、异冰片以及布洛芬衍生物,天然产物如香茅醇、植物醇、紫苏醇以及香芹醇的衍生物也都能够顺利进行该反应(图2)。值得注意的是,该反应在较低CO2浓度氛围下也可以进行(30% CO2 in Ar),对CO2在有机合成化学中的应用具有重要的参考意义(图3)。

▲图3. 低浓度CO2实验
理论计算结果表明:萘自由基负离子作为反应过程中的中间体,经单电子转移还原卤化物在能量上是非常有利的,紧接着生成的卤化物自由基负离子快速发生解离,生成相应的芳基或者烷基自由基。接着,作者通过循环伏安法(CV)实验进行了反应机制的研究。首先,在氩气氛围下,观察到了底物3在-3.53 V vs Ag/AgNO3的还原峰(图4a,红线);在-3.09 V vs Ag/AgNO3观察到了萘的可逆还原峰(图4a,蓝线)。当向萘中加入底物后,萘的还原峰明显增大,证明了该过程中有催化电流。该结果表明萘可以作为媒介促进卤苯的还原。接着,作者还尝试逐渐增大体系中底物的浓度,可以明显地观察到萘的氧化峰逐渐消失,还原峰逐渐增大,且当底物的浓度增大到萘的3.5倍时,萘的氧化峰完全消失(即体系中萘的量约为30%)(图4b)。这一结果与实验一致,即萘的量为30 mol%为最优条件。此外,以60作为底物时,将温度降到0 ℃,标准条件下生成了相应的分子内环化羧化的产物,证明了反应过程中芳基自由基的存在(图4c)。
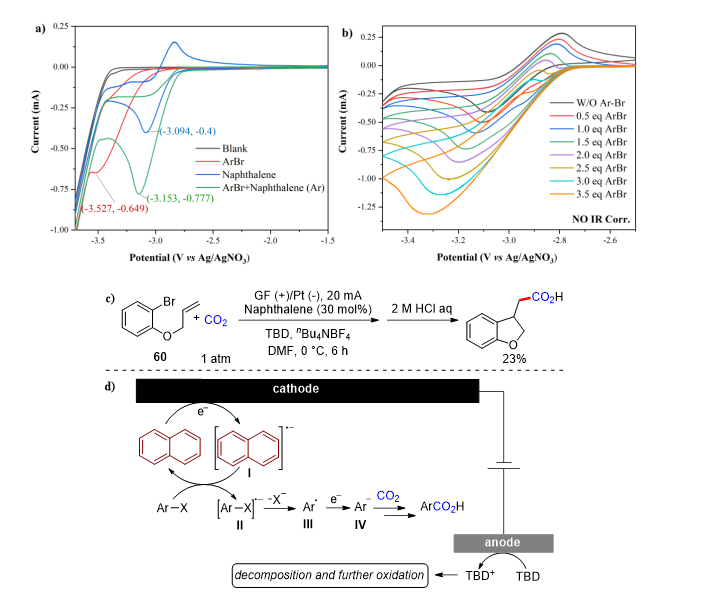
▲图4.反应机理研究
根据机理研究和文献报道,作者提出了可能的反应机理(图4d):萘在阴极被还原成萘自由基负离子,萘自由基负离子经单电子转移将卤化物还原成卤化物自由基负离子II,紧接着II发生解离生成自由基中间体III,III继续被还原生成中间体IV,紧接着中间体IV对CO2进行亲核进攻。最后,酸化得到目标产物。
01 小结
仇友爱课题组发展了一种新型有机还原媒介促进的碳卤键电化学羧化的方法,萘作为廉价易得的有机媒介,CO2作为绿色经济的羧基源;对不同的官能团都表现出良好的耐受性;可以兼容天然产物、药物分子及其衍生物的后修饰结构。相关成果发表在Angewandte Chemie International Edition上。该工作得到了中央高校基本科研业务费及南开大学有机新物质创造前沿科学中心专项资金的支持。理论计算部分由中科院上海有机所薛小松研究员完成。特别感谢周其林老师的大力支持和鼓励。南开大学化学学院仇友爱研究员为第一通讯作者,博士后王衍伟为文章第一作者。
原文:
Metal-Free Electrochemical Carboxylation of Organic Halides inthe Presence of Catalytic Amounts of an Organomediator, Yanwei Wang, Zhiwei Zhao, Deng Pan, Siyi Wang, Kangping Jia, Dengke Ma, Guoqing Yang, Xiao-Song Xue* and Youai Qiu*, Angew. Chem. Int. Ed. 2022, DOI: 10.1002/anie.202210201.
02 作者简介
仇友爱,南开大学化学学院特聘研究员、博士生导师、独立课题组组长(PI),南开大学“百名青年学科带头人”,入选国家高层次人才青年项目。2015年6月博士毕业于浙江大学化学系,师从于麻生明教授。2015年9月加入瑞典斯德哥尔摩大学Jan-Erling Bäckvall教授课题组从事博士后研究。2017年9月加入德国哥廷根大学Lutz Ackermann教授课题组从事博士后研究。2019年11月起,获日本学术振兴会特别研究员奖学金(JSPS Fellowship),作为访问研究员加入日本理化学研究所(RIKEN)侯召民主任研究员课题组。2020年9月底入职南开大学化学学院元素有机化学国家重点实验室,开始独立研究工作,主要开展绿色有机合成研究,特别是有机电化学的研究。长期从事过渡金属催化的有机电化学、过渡金属催化的有机合成化学、主族元素化学及小分子电化学转化等。以通讯作者及第一作者发表学术论文30余篇,含Acc. Chem. Res. (1篇),J. Am. Chem. Soc. (4篇),Angew. Chem. Int. Ed. (9篇),Nat. Comm.(1篇),CCS Chem. (1篇)。
仇友爱课题组网站:
https://www.x-mol.com/groups/qiu_youai
仇友爱课题组热诚欢迎师资博士后、博士和硕士研究生加盟,有意者请和仇老师联系:qiuyouai@nankai.edu.cn




