来源:CCSChemistry
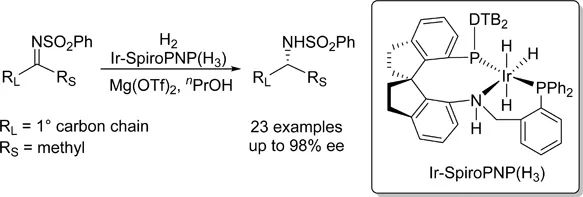
近日,南开大学周其林团队通过对其课题组发展的铱-手性螺环膦-氮-膦催化剂的空间位阻精准调节,以高产率和高对映选择性实现了双烷基亚胺不对称氢化反应。
背景介绍:
手性胺是许多天然产物和药物中的重要结构。因此,手性胺的合成备受化学家们的关注。在各种手性胺合成方法中,亚胺的不对称氢化反应以其高原子经济性成为最有效的方法之一。高效催化剂的开发是亚胺不对称氢化反应成功的关键。过去二十年中发展的催化剂主要适用于芳基-烷基亚胺和环状亚胺的不对称氢化反应,而用于双烷基亚胺氢化的催化剂却较为罕见。双烷基亚胺不对称氢化的主要挑战在于手性催化剂对性质相似的双烷基的有效识别。
本文亮点:
最近,南开大学周其林教授团队发展了一种手性螺环膦-氮-膦配体的铱催化剂。在这篇文章中,他们通过精准调控催化剂手性空腔和底物上亚胺保护基,并通过一系列反应条件的优化,发现以C4为催化剂可以实现双烷基亚胺的高对映选择性氢化(图1)。
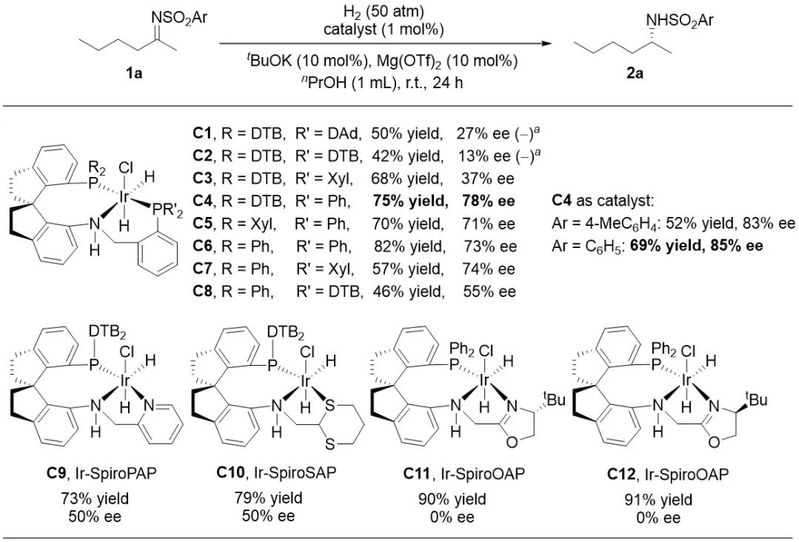
图1. 催化剂设计
随后,作者考察了一系列双烷基亚胺底物的普适性(图2)。烷基链的长度对产率和对应选择性没有影响(2a-2d),增加烷基取代基的位阻,对映选择性有所提高(2e-2g)。值得一提的是,甲基和乙基在空间上和电性上都非常相似,因此2-丁酮亚胺的催化不对称氢化极具挑战性。作者使用C4(H3)作为催化剂,能够以81% ee将2-丁酮亚胺氢化为相应的手性胺。另外,这个催化体系有很好的官能团兼容性。
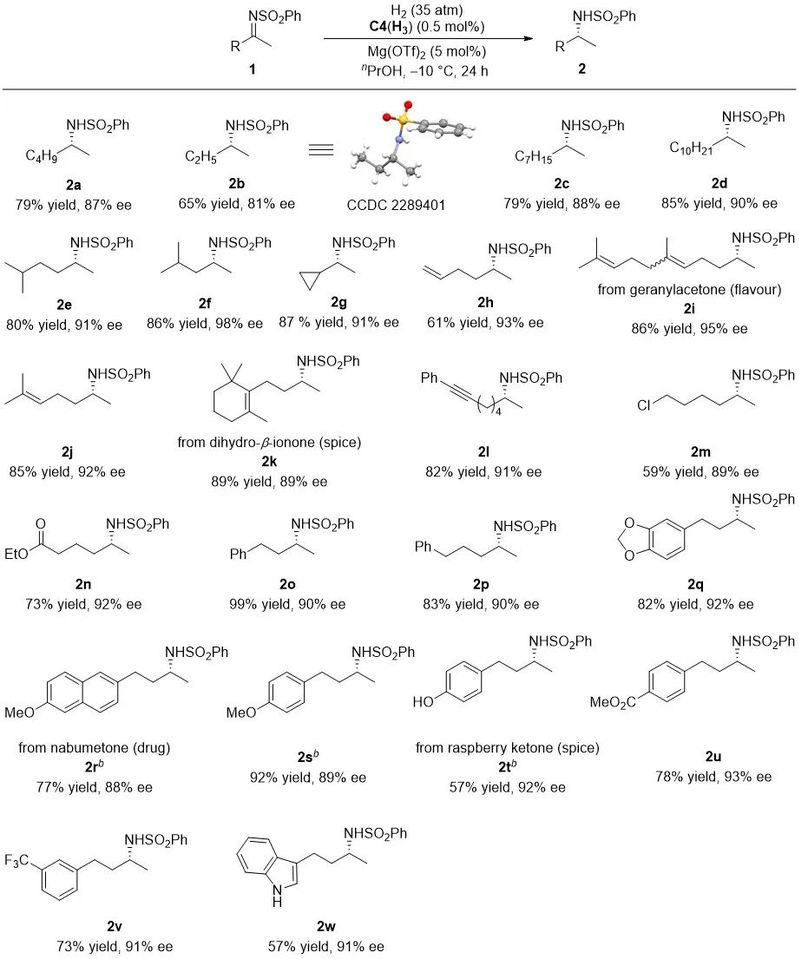
图2. 底物适用范围
为了进一步展示该方法的实用性,作者进行了克级规模实验和产物转化实验(图3)。在克级实验中,反应的收率及对映选择性能够保持(97% yield, 92% ee)。随后,作者使用Li/naphthalene顺利将保护基脱除,得到了手性药物(R)-Isometheptene。
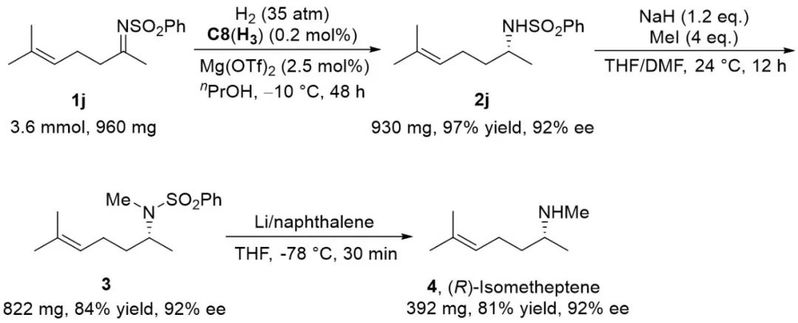
图3. 克级规模实验和产物转化
为了解释催化剂在反应中如何控制对映选择性,作者对反应过程进行了DFT计算。通过结构优化,作者得到了催化剂C4(H3)的最优结构(图4a)。基于酮氢化中Noyori提出的双功能催化机理模型,作者假设了一个六元环过渡态I(图4b)。然而,由于螺环骨架的刚性和非常拥挤的催化剂空腔,带有磺酰基的亚胺,很难以六元环过渡态与催化剂结合。进一步的计算结果表明,反应可能存在一个类似的八元环过渡态II(图4b)。对过渡态II的计算结果显示,S产物的过渡态TSS比R产物的过渡态TSR高1.8 kcal mol-1,这与实验结果相吻合。从催化剂C4(H3)的包埋体积图中可以看出,P2上的3,5-二叔丁基苯基、P1的苯基和螺环骨架共同组成了一个拥挤的手性口袋。当亚胺底物以Si前手性面靠近催化剂活性中心时,磺酰基、甲基和乙基能与催化剂手性口袋精准匹配。这些计算结果很好地解释了C4(H3)具有高对映选择性的原因。
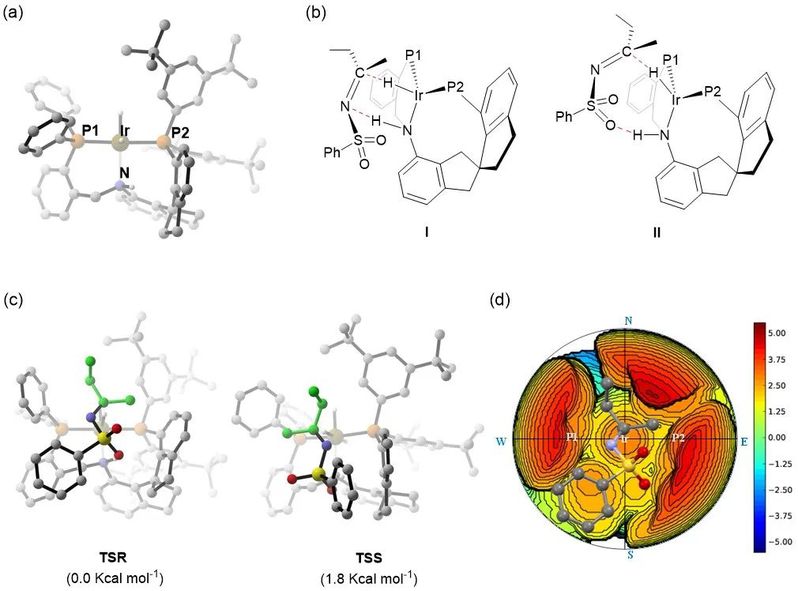
图4. DFT理论计算
总结与展望:
作者通过对手性螺环膦-氮-膦配体位阻的精准调节,设计合成了一个具有拥挤手性口袋的催化剂C4(H3)。该催化剂可以有效识别亚胺的两个烷基,氢化双烷基亚胺,为手性胺的不对称合成提供了一个高效、高对映选择性方法。
该工作以Communication的形式发表在CCS Chemistry上。第一作者为南开大学博士研究生王峥。
文章详情:
Iridium-catalyzed Asymmetric Hydrogenation of Dialkyl Imines
Zheng Wang, Xin-Yi Yang, Yue Xu and Qi-Lin Zhou*
Cite this by DOI:
10.31635/ccschem.023.202303600
文章链接:
https://doi.org/10.31635/ccschem.023.202303600




