
第一作者:汤士标
通讯作者:王佰全教授
单位:南开大学
背景
吡啶骨架广泛存在于药物活性分子、配体和功能材料中,尤其在药物化学领域,围绕吡啶骨架的官能化反应受到合成化学家的广泛关注。近年来,后期C-H键官能化反应的发展丰富了吡啶官能化的策略,然而,吡啶骨架的后期羧基化是一个长期存在的挑战,这也大大限制了新型吡啶羧酸类化合物的合成与开发。
二氧化碳作为一种无毒、廉价、可再生的绿色C1资源,以CO2作为羧基源,开发吡啶骨架的选择性羧基化反应在合成化学领域具有显著的吸引力。然而,由于吡啶环具有缺电子性,而且二氧化碳热力学稳定性高,动力学惰性,将CO2高效插入至吡啶骨架具有极大的挑战,尤其是对一些复杂的吡啶药物分子,其与CO2的选择性羧基化反应始终未被实现。
工作介绍
本工作首次实现了复杂吡啶分子骨架与CO2的后期C4-H键羧基化反应,同时也是首例C-P键与CO2直接羧化反应的报道。该反应以廉价的铜盐为催化剂,可以在室温、1标准大气压CO2的条件下对比沙可啶、氯雷他定等吡啶药物分子骨架实现选择性羧基化修饰。相较于文献报道的CO2参与的直接羧化反应,该体系展现出了优异的官能团耐受性与底物范围性,同时操作便捷,容易放大,在吡啶类新药设计与开发领域展现出了显著的应用潜力。
该成果以《Copper-Catalyzed C4-selective Carboxylation of Pyridines with CO2 via Pyridylphosphonium Salts》为题发表在国际化学顶级期刊《Angewandte Chemie International Edition》上,博士生汤士标为文章第一作者
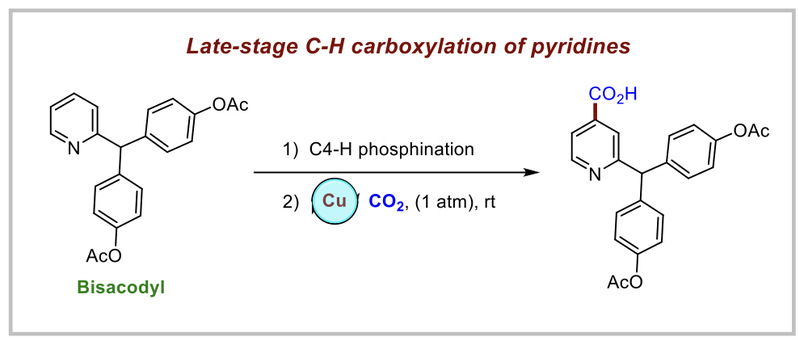
图1. 铜催化芳基噻蒽鎓盐与CO2的羧基化反应
通过对配体、还原剂和溶剂等条件的筛选,作者选择了以廉价易得的四甲基乙二胺为配体,二乙基锌为还原剂的标准反应体系。在最优条件下,除了常规的含取代基的吡啶底物,包含C-Br键、C-Cl键、烯基、炔基、酯基、氰基等高活性取代基的底物也展现出良好的兼容性。相较于目前报道的碳杂键与CO2的羧化反应,该体系的官能团耐受性具有显著优势。此外,该体系还实现了对紫檀芪衍生物、氯雷他定、比沙可啶等复杂的吡啶药物骨架的C4选择性羧基化修饰,为异烟酸类化合物的开发提供了一种新策略。
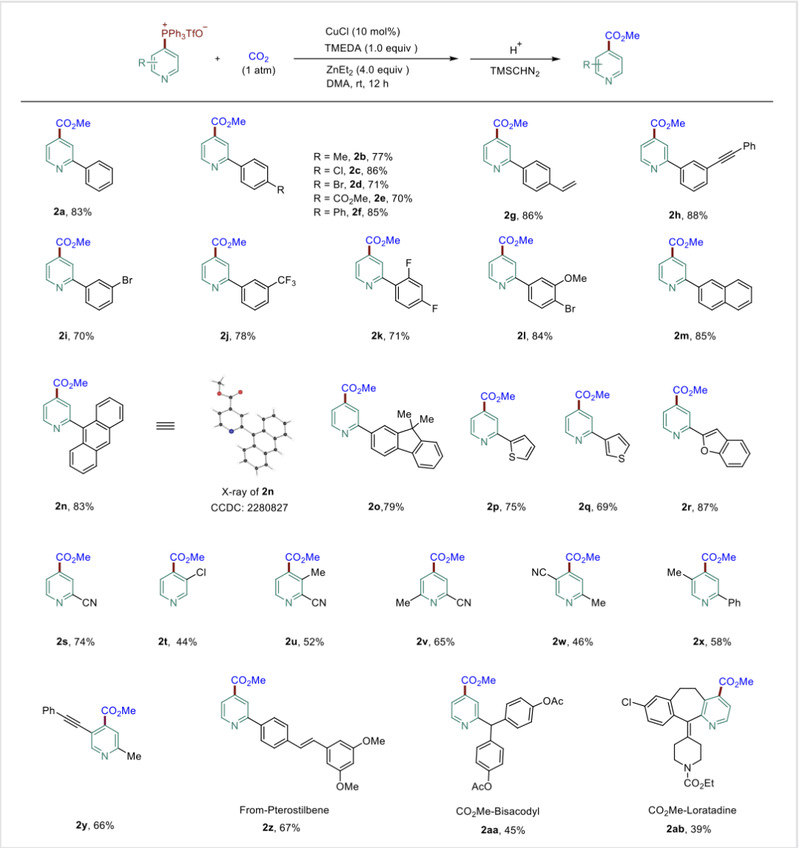
图2. 底物适用范围
接着,作者直接从吡啶化合物出发,以克级规模一锅法高效得到了羧化产物。基于该体系优异的官能团耐受性,产物可以实现Suzuki偶联、二氟环丙烷化、酯化等衍生化转化,证明了基于该反应进一步拓展异烟酸类新化合物的可能。
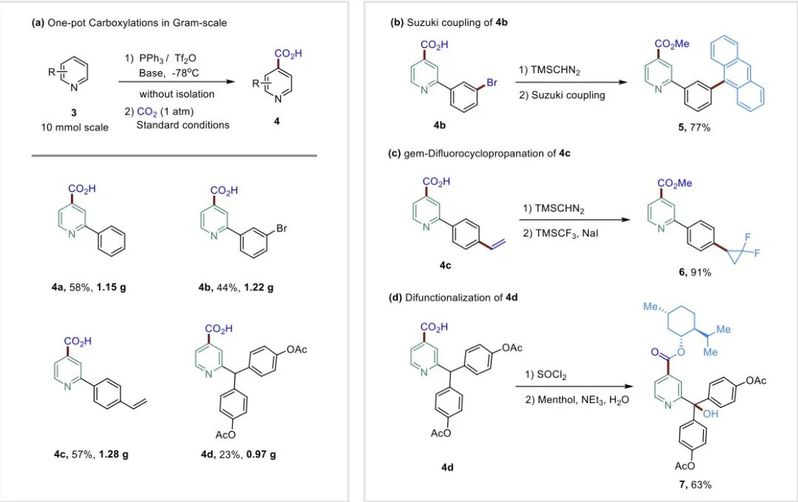
图3. 串联放大实验与应用转化
在反应机理方面,通过自由基捕获、活性中间体探索、气体检测等一系列机理实验,作者提出了由活性零价铜启动,经单电子转移得到一价吡啶铜物种,继而进行直接CO2插入的反应机理。反应中可能存在铜锌转金属化作用,生成吡啶锌试剂,但吡啶锌试剂在室温下只有很弱的羧化能力,因此,吡啶铜物种的生成是该反应室温下高效进行的关键。
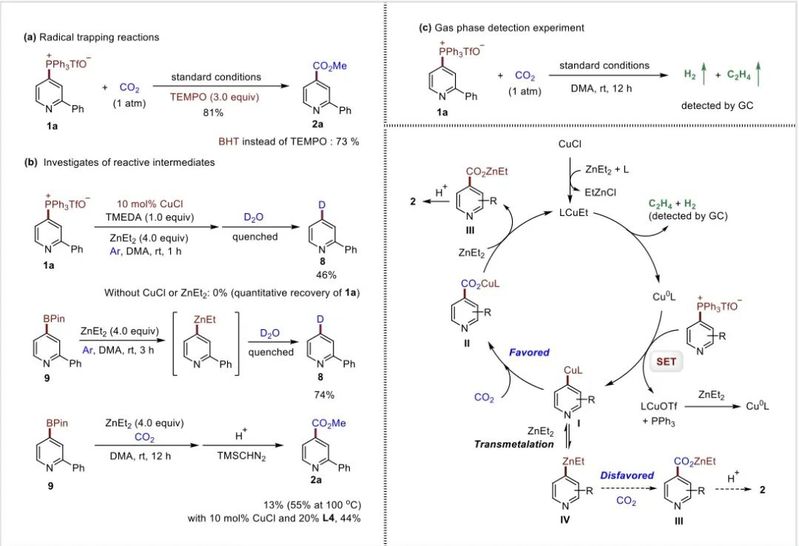
图4. 反应机理研究
总结
在该工作中,王佰全教授课题组实现了吡啶化合物与CO2的C4选择性羧基化反应,反应采用廉价铜催化剂,条件温和,具有优异的官能团耐受性与底物普适性,反应容易放大,操作便捷,为异烟酸类药物的设计与开发提供了一种简洁高效的合成方法。此外,在碳杂键与CO2的直接羧化领域,该工作实现了首例C-P键与CO2的直接羧化,开发了一种羧化反应新模式。对于喹啉、吡嗪等杂环骨架,该体系仍有一些局限性,这些含氮杂环骨架与CO2的选择性羧化反应有待进一步探索。
原文:
Copper-Catalyzed C4-selective Carboxylation of Pyridines with CO2 via Pyridylphosphonium Salts.
Angew. Chem. Int. Ed. 2024, e202318572
Shibiao Tang, Zezhao Liu, Jiakai Zhang, Bin Li, Baiquan Wang*
First published: 02 February 2024 | https://doi.org/10.1002/anie.202318572.
王佰全课题组网站:
https://www.x-mol.com/groups/Wang_Baiquan
http://skleoc.nankai.edu.cn/info/1018/4487.htm




