来源:高分子科技
自然界中生物分子的识别过程使其能够自下而上组装形成功能各异的生物学结构。例如在细胞骨架中,微管和微丝分别由微管蛋白和肌动蛋白通过自我识别聚集形成不同的纤维结构,这种多重物种间识别作用称为自分类(self-sorting),即分子在复杂体系中有效地区分自我与非我,并选择性地进行识别的过程。尽管目前已经成功开发了多种人工自分类系统,但由于生物体内不同分子的运输和新陈代谢存在显著差异,特别是不同组装基元由于它们组装过程的差异性以及系统性给药后的生物分布不确定性,在体内实现人工合成分子的自分类组装依然面临挑战。
针对该挑战,南开大学余志林课题组在《J. Am. Chem. Soc.》期刊上以“In Vivo Self-Sorting of Peptides via In Situ Assembly Evolution”为题(DOI: 10.1021/jacs.4c10309),报道了一种基于原位组装体衍变的活体多肽自分类组装体系。该多肽分子由双硫键共价连接的自分类组装基元构成,能自组装形成短纳米棒状结构。以肿瘤细胞过表达谷胱甘肽(GSH)为刺激源,诱导多肽发生双硫键切割,同时释放两个组装基元,启动多肽原位组装衍变、构筑自分类组装体系。以肿瘤细胞细胞器内质网以及凋亡抑制蛋白XIAP为治疗靶点,通过非共价共组装手段,分别引入靶向内质网和XIAP蛋白的配体单元,通过在细胞内形成自分类组装结构引起内质网功能性障碍和提高细胞凋亡水平,从而实现活体肿瘤的联合治疗。

图1. 基于原位多肽组装体演变的活体多肽自分类组装体系及其肿瘤联合治疗。图片来源J. Am. Chem. Soc.。
在前期胞内多肽自分类组装(J. Am. Chem. Soc. 2022, 144, 9312-9323.)的工作基础上,余志林团队通过二硫键共价连接两种具有不同组装模式的自分类组装基元E3C16SH和SHEIY,设计合成了具有组装能力的自分类组装前体E3C16-SS-EIY。其中,E3C16SH通过疏水C端穿插组装形成超螺旋纳米带,而SHEIY以哑铃型两亲性结构组装形成扁平纳米带,共价连接通过破坏它们原有的自分类组装结构从而实现在肿瘤组织内GSH切割,同时释放两组自分类组装基元的目的。在此基础上,通过共价连接的方式分别在多肽E3C16-SS-EIY序列N端引入XIAP蛋白靶向基团Smac肽(AVPIAQK)以及C端引入具有内质网靶向性的对甲苯磺酰胺(Ts)构建多肽配体L4。将L4与多肽E3C16-SS-EIY进行非共价共组装得到多肽共组装体E3C16-SS-EIY+L4。E3C16-SS-EIY+L4通过肿瘤原位GSH还原后形成自分类组装体E3C16SH+L1和SHEIY+L2,分别形成左手螺旋和扁平纳米带来结合XIAP蛋白和破坏内质网稳态从而诱导Caspase-3蛋白和GRP78蛋白表达上调导致肿瘤细胞凋亡和ER功能性障碍来达到联合治疗的效果。
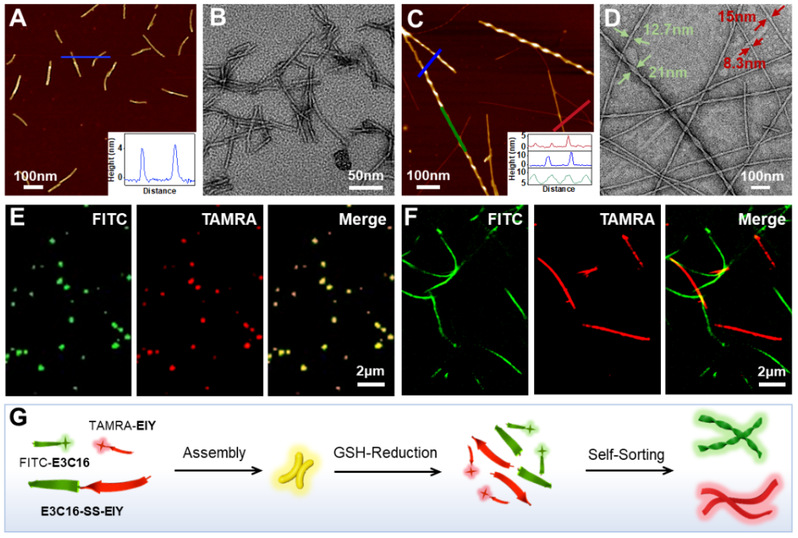
图2. 多肽自分类组装前体E3C16-SS-EIY在GSH响应前后的组装体形貌和自分类组装表征。
溶液中的GSH响应型组装形貌表明多肽E3C16-SS-EIY在GSH响应前组装形成短纳米棒,在GSH还原后形成左手螺旋和扁平纳米带,并形成了有效的自分类组装。并且通过激光共聚焦和MST实验,成功验证了E3C16-SS-EIY+L4具有同时结合肿瘤细胞XIAP蛋白和靶向ER,并激活依赖于Caspase的细胞凋亡途径和诱导ER功能障碍导致细胞死亡。通过共聚焦成像验证了多肽E3C16-SS-EIY在肿瘤细胞和肿瘤活体内成功发生了原位自分类组装。并且活体治疗研究表明,自分类组装前体具有良好的肿瘤积累和保留效果,以及在与化学药物CPT联合给药时具有良好的生物安全性和抑制肿瘤生长的能力。该工作开发了一种新型体内多肽自分类组装体的治疗系统,为高效生物药剂的体内原位构筑拓展了一种新思路。
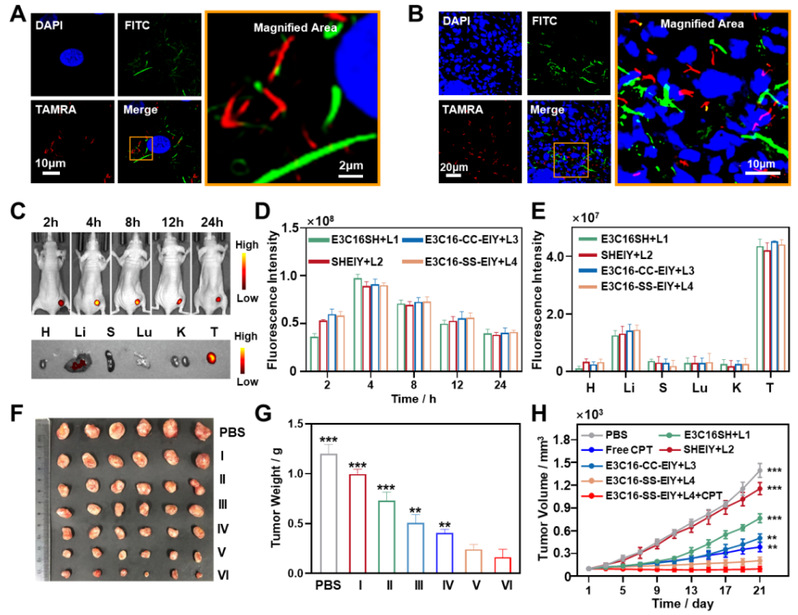
图3. 多肽自分类组装前体E3C16-SS-EIY的肿瘤细胞/活体自分类成像以及体内肿瘤治疗疗效。
这一成果近期发表在J. Am. Chem. Soc.上。文章第一作者为南开大学化学学院高分子化学与物理专业博士研究生刘欣,南开大学余志林教授为通讯作者。该研究得到科技部纳米前沿重点专项项目、国家自然科学基金委、合成生物学海河实验室以及物质绿色创造与制造海河实验室等项目的资助。
原文链接:
https://pubs.acs.org/doi/10.1021/jacs.4c10309




