黄有教授、肖力军研究员Angew:膦催化联烯酸酯的跨环环化实现对映选择性[2+2]双环合成
2025-12-19
来源:化学深耕堂
深耕点评
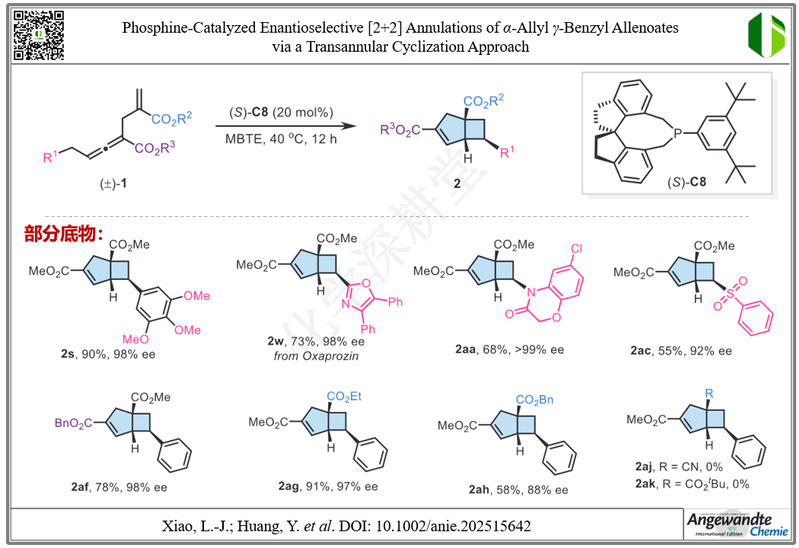
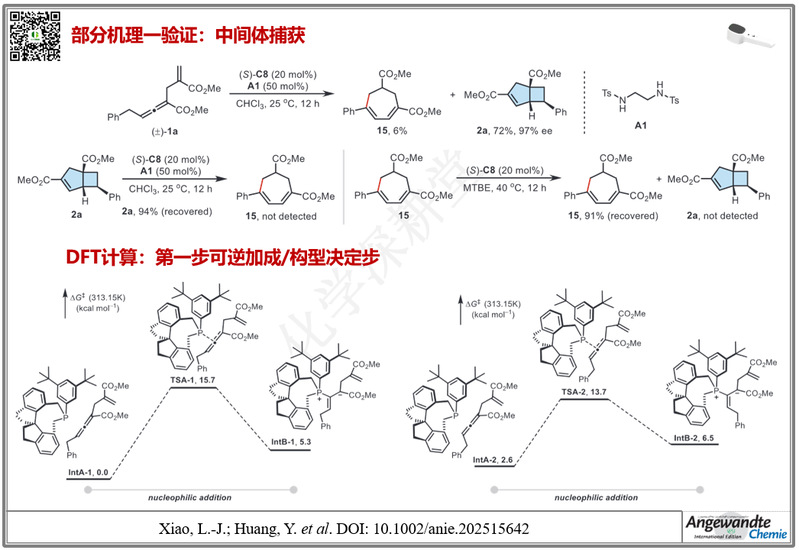
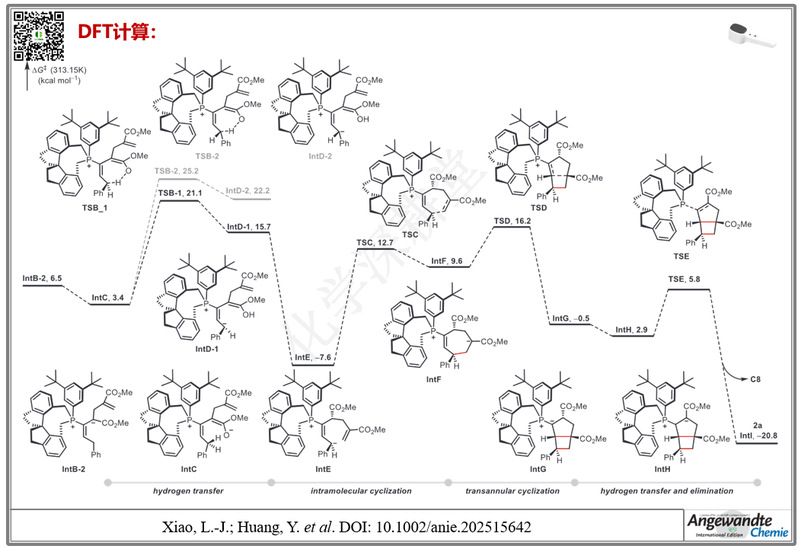
近日,南开大学黄有/肖力军课题组开发了一种由手性螺环膦催化的对映选择性[2+2]环加成反应,以外消旋α-烯丙基-γ-苄基联烯酸酯为底物,通过形成七元环中间体并经历跨环(transannular)环化,高效构建含有四元环的双环bicyclo[3.2.0]结构。该策略:1. 能够构建含有三个连续手性中心的张力型双环骨架,产物可作为间位与对位取代苯环的生物电子等排体,展现重要的结构与应用价值。2. 螺环膦催化剂提供高度刚性的手性环境,使外消旋底物在反应中实现立体收敛,表现出优异的对映选择性和底物普适性。3. 机理研究结合同位素交换、添加剂捕获、产物ee随时间变化及DFT计算揭示:反应的第一步膦对联烯酸酯的亲核加成是可逆的,这一可逆性使两个对映体不断互相转化,从而实现动态动力学拆分(DKR);随后,位于δ-碳的氢通过分子内部的氢转移被去除,这一步不仅决定了反应的速度,也直接控制了最终产物的立体构型;之后的跨环环化步骤能顺利进行,对产物的立体选择性影响较小。
文献信息
Phosphine-Catalyzed Enantioselective [2+2] Annulations of α-Allyl γ-Benzyl Allenoates via a Transannular Cyclization Approach
Xu-Ling Pan, Wei-Guo Xiao, Li-Jun Xiao*, Qi-Lin Zhou and You Huang*
Angew. Chem. Int. Ed. 2025, DOI: 10.1002/anie.202515642




