来源:量化与第一性原理笔记

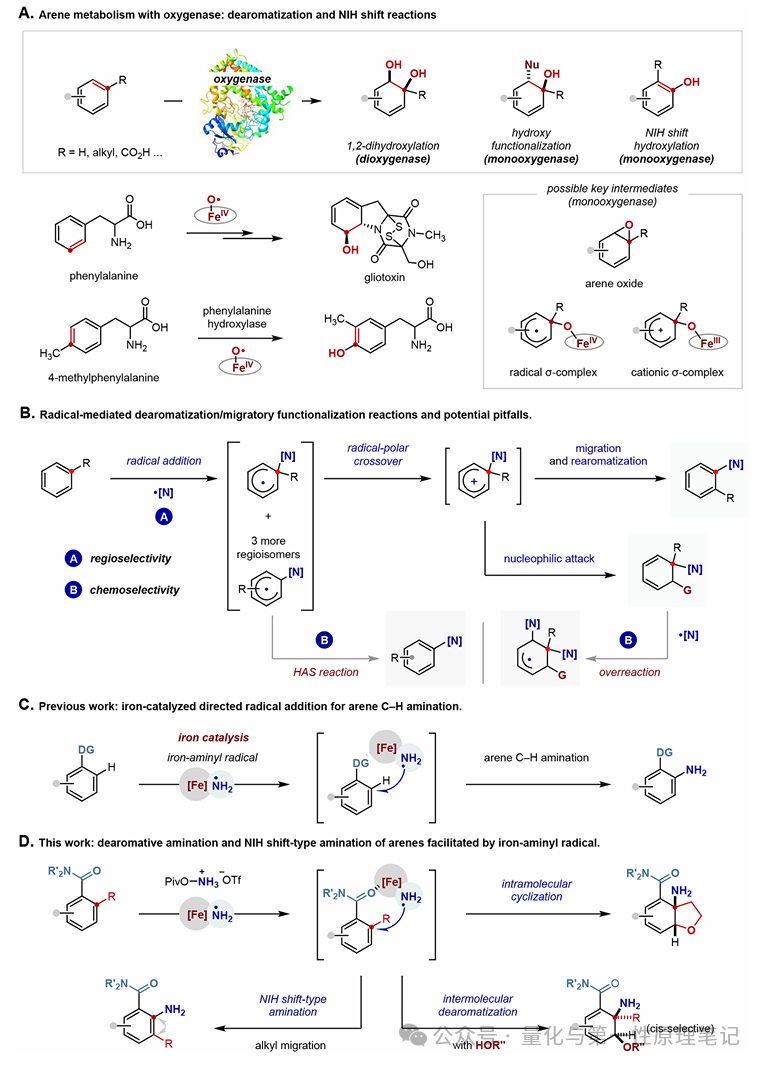
加氧酶催化的芳烃氧化转化是生物体中芳香族化合物的核心代谢途径,其固有的羟基化脱芳构化和芳烃羟基化反应已成功应用于有机合成。而含氮官能团在生物活性分子中普遍存在,但构建有价值C−N键的芳烃代谢途径氮杂类似物,在酶系统和仿生催化中仍难以实现。开发铁催化介导的芳烃氮杂代谢转化反应,对丰富C−N键形成合成工具、连接天然代谢过程与仿生催化具有重要意义。
近日,南开大学王飞教授课题组通过以 O - 保护的三氟甲磺酸羟胺为胺化试剂,Fe (OAc)₂为催化剂,实现分子内和分子间的氨基 - 醚化反应。该反应能够高选择性生成 1,3 - 环己二烯产物,烷氧基选择性结合在 C3位且与氨基呈顺式结构(dr>10:1)。底物适用范围广,为 C−N 键构建提供了新的方法。
01 核心问题
1. 如何利用铁-胺基自由基模拟加氧酶的铁-氧核心,实现芳烃的脱芳构化胺化和NIH迁移型胺化?
2. 如何解决芳烃底物自由基捕获的区域选择性差、脱芳构化反应中σ-复合物易再芳构化、产物易过度反应等关键挑战?
3. 该铁催化胺化反应的机理、底物适用范围及在复杂分子合成中的应用价值?
02 研究方法
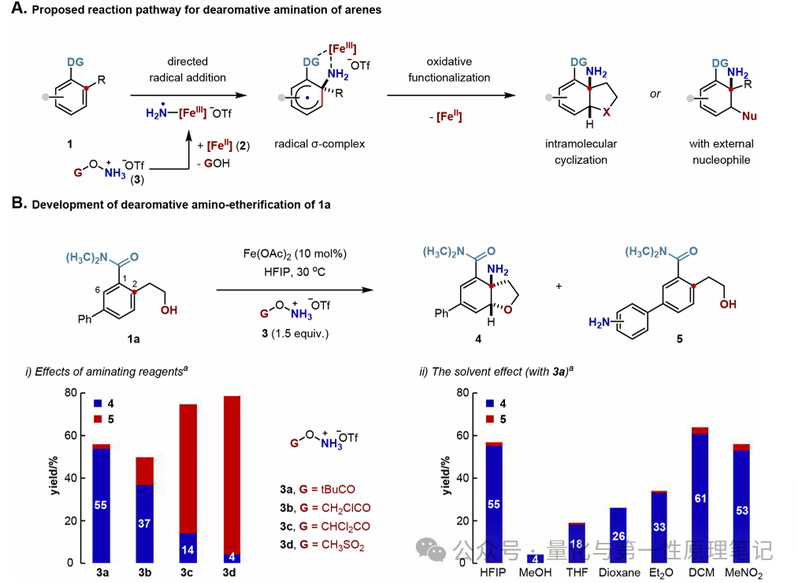
1. 反应体系优化:以苯甲酰胺为底物、O-保护的三氟甲磺酸羟铵为亲电胺化试剂,筛选催化剂(乙酸亚铁)、溶剂(HFIP、DCM等)、胺化试剂、温度及反应时间等关键条件,确定最优反应参数。
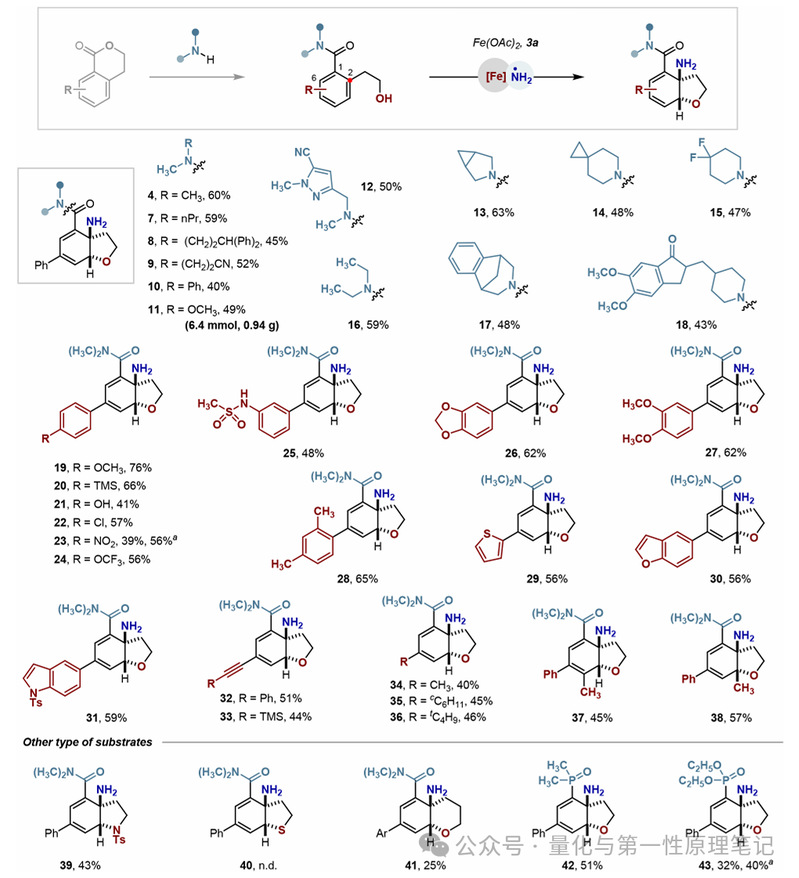
2. 底物范围拓展:系统考察含不同取代基(给电子/吸电子基团、杂环、炔基、烷基等)的苯甲酰胺类底物,以及不同导向基团(酰胺、氧化膦、磷酸酯)的兼容性。
3. 机理验证与计算:通过电子顺磁共振(EPR)光谱、自由基钟实验等控制实验,结合密度泛函理论(DFT)计算,探究反应路径;分析σ-复合物的形成与转化过程。
4. 实用性验证:开展产物后续转化(如酰胺化、磺酰胺化、[4+2]环加成、杂环合成)及放大反应,验证方法的应用价值。
03 主要内容
1. 反应特性与底物兼容性:
脱芳构化胺化反应:选择性生成1,3-环己二烯产物,兼容噻吩、苯并呋喃、吲哚等杂环及三甲基硅基、羟基、氯、硝基等官能团,可实现分子内和分子间氨基醚化反应,产物中烷氧基与氨基呈顺式构型(dr>10:1)。
NIH迁移型胺化反应:实现烷基、氘、氢化物迁移,从单一苯甲酰胺底物同时获得2-苯胺基苯甲酰胺的构造异构体,联合产率最高达91%,溴原子等官能团可耐受。
导向基团拓展:除酰胺外,氧化膦和磷酸酯也可作为合适的导向基团,获得脱芳构化产物。
2. 反应机理:
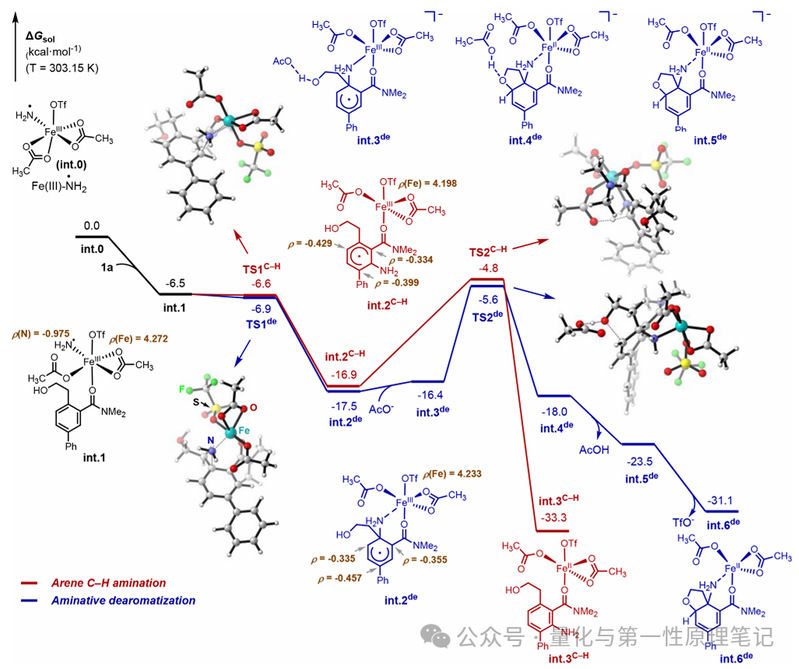
脱芳构化胺化:乙酸亚铁与胺化试剂发生单电子转移生成铁(III)-胺基自由基,底物与该自由基螯合后发生导向自由基加成形成σ-复合物,进而经氧化官能化生成脱芳构化产物;DFT计算证实脱芳构化路径在能量上略占优势(ΔΔG‡=0.8 kcal·mol⁻¹)。
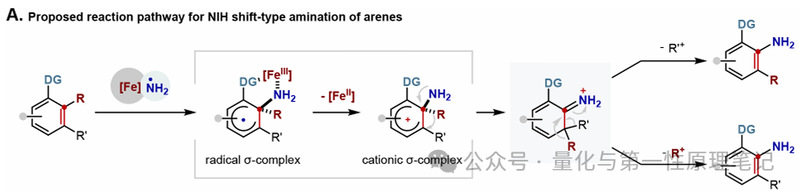
NIH迁移型胺化:自由基σ-复合物经自由基-极性交叉形成阳离子σ-复合物,随后发生取代基迁移生成亚胺中间体,再芳构化得到苯胺类产物。
3. 方法优势与应用:
反应条件温和(室温或0℃、无需额外氧化剂),区域选择性高,底物范围广;
产物可通过酰胺化、磺酰胺化、环加成等反应高效转化为多种复杂结构,2-苯胺基苯甲酰胺产物可进一步合成喹唑啉二酮、喹唑啉酮等药物相关杂环;
Weinreb酰胺底物可实现6.4 mmol规模放大反应,产率保持49%。
04 总结
本研究首次实现了铁-胺基自由基介导的苯甲酰胺脱芳构化氨基醚化和NIH迁移型胺化反应,模拟了加氧酶的铁-氧核心功能。
该方法具有区域选择性高、反应条件温和、底物范围广、产物转化多样等优势,控制实验与DFT计算明确了反应机理。该反应不仅拓展了C−N键形成的合成方法,还填补了天然代谢过程与仿生催化之间的空白。




