来源:南开化学
蛋白质中氨基酸残基的手性异构化现象,包括L型向D型转变以及Asp向isoAsp异构化等,被认为与蛋白质老化、构象变化及部分神经退行性疾病过程相关。由于这类异构体通常具有相同分子量和相近化学组成,传统质谱方法较难对其进行直接区分,因此长期以来缺乏适用于复杂样本的系统分析手段。围绕这一问题,南开李功玉团队近年来在分析方法建立、蛋白质组尺度识别及疾病相关机制研究等方面开展了持续研究,取得了系列进展(Anal. Chem. 2023/2025;Angew. Chem. 2023/2026;PNAS 2026; Sci. Adv. 2026)。
近日,南开大学李功玉教授研究团队在阿尔茨海默病(Alzheimer's disease, AD)分子机制研究方面取得新进展。该团队将自主开发的、具有自主知识产权的手性蛋白组学(Stereoproteome, STEP)技术流程应用于临床AD患者脑组织样本中淀粉样蛋白(Aβ42)手性变体的鉴定与构效关系分析,探讨了特定D-型氨基酸异构体与原生L-型Aβ42之间的“串扰效应(Crosstalk)”及相关的神经保护机制。相关研究成果以《Clinically Relevant Stereochemistry Reprograms Amyloid Proteome for Aggregation Crosstalk-conferred Neuroprotection》为题发表于学术期刊《Science Advances》。该研究论文的第一作者为南开大学化学学院2022级直博士周佳欣,通讯作者为李功玉研究员。研究团队得到了多位专家的技术支持,包括南开大学化学学院余志林教授、天津医科大学郑珍教授,以及南开大学王倩倩和刘宁老师等。关键质谱数据在“药物化学生物学全国重点实验室”和“物质绿色创造与制造海河实验室”结构质谱平台完成采集。该研究获得了国家重点研发计划青年科学家项目、天津市自然科学基金重点项目等经费支持。
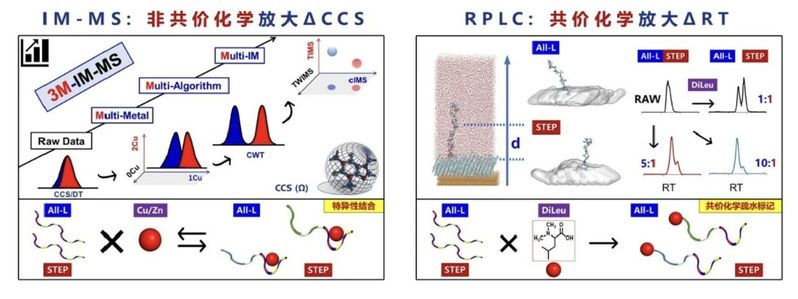
图1、手性构型差示放大策略:A)非共价特异性金属结合用于离子淌度质谱手性构型差异放大;B)共价化学疏水标记用于反相色谱手性构型差异放大。
李功玉长期从事蛋白手性质谱分析相关研究。在方法学方面(图1;Anal. Chem. 2023/2025),针对蛋白手性变体“质量相同、结构差异细微、丰度较低、缺乏通用富集标记”等分析难点,团队逐步建立了结合液相色谱、离子迁移质谱、多维信号解析和计算算法的研究路径。相关工作利用离子迁移质谱对构象差异较为敏感的特点,引入金属离子配位、构象差异放大等策略,并结合连续小波变换、高斯拟合等信号处理方法,提高了对D-氨基酸取代和Asp/isoAsp异构化等立体差异的分辨能力。在此基础上,团队进一步发展了STEP非靶向搜索流程,将保留时间偏移、碰撞截面积差异、序列引导搜索、机器学习评分等信息纳入统一分析框架,并结合标准品加标和酶学验证等手段提升鉴定可信度。上述工作为蛋白手性异构体的规模化识别提供了方法基础(图2;Anal. Chem. 2025,授权中国发明专利2项+转件著作权1项)。
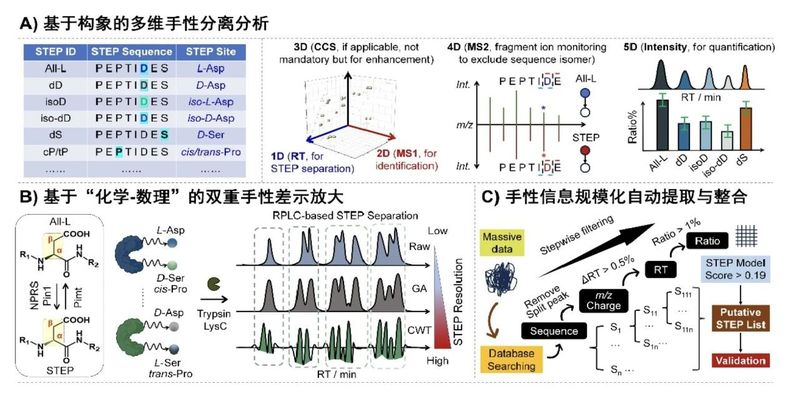
图2、手性分辨蛋白质组学方法体系关键策略:A) 基于构象的多维手性分离分析;B) 基于“化学-数理”的双重手性差示放大;C) 基于机器学习的手性信息规模化自动提取与整合。
在蛋白质组尺度研究方面,团队将相关分析方法应用于神经退行性疾病相关细胞模型,开展了手性异构体的非靶向识别研究,发现了一批具有手性异构特征的肽段及潜在相关蛋白,并通过标准品、酶切实验和统计评分等多种证据对部分结果进行了验证。相关研究表明,蛋白手性异构化可能在细胞蛋白组中具有一定广泛性,其丰度和分布特征具有进一步分析价值(Anal. Chem. 2025)。与此同时,团队还对液相色谱-离子迁移质谱联用、金属离子复合、寡聚化放大及多算法联合解卷积等技术路线进行了系统总结和拓展,为后续在组织样本、疾病样本及临床样本中开展更大范围研究提供了技术参考(Anal. Sens. 2025;《质谱学报》2022a/b)。
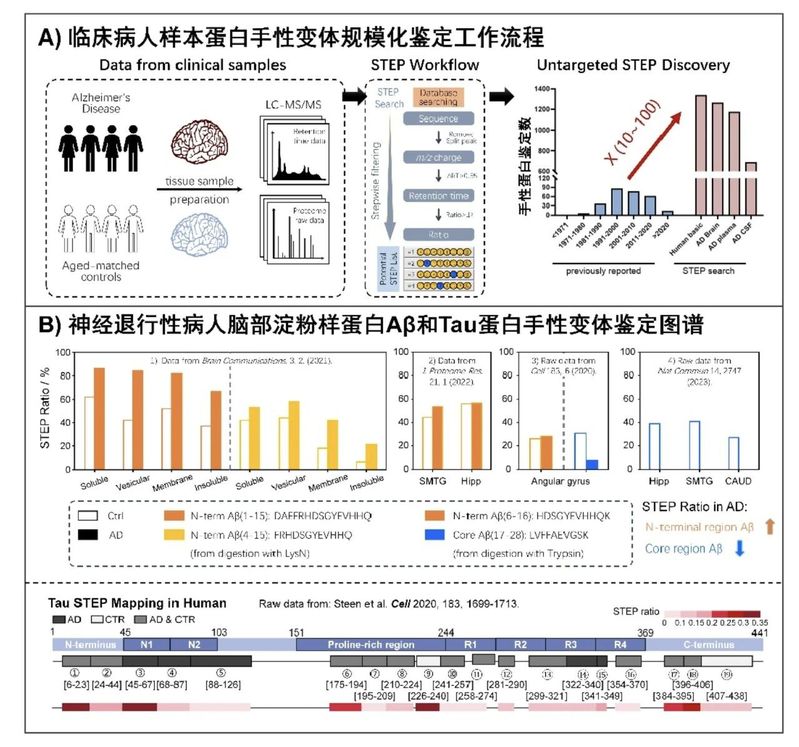
图3、临床样本蛋白手性化学图谱绘制:A) 临床样本蛋白手性变体规模化鉴定工作流程,将手性蛋白异构体的鉴定数量提升1-2个数量级;B) AD病人脑部Aβ42和Tau手性变体含量分布图
利用自主开发的手性蛋白组质谱方法,南开李功玉团队率先绘制了阿尔茨海默病患者脑组织中 Aβ42 和 Tau 蛋白的手性异构图谱(图3;Sci.Adv.2026),揭示了 Aβ42 在AD脑组织中的结构域特异性的手性异构规律:N 端柔性区 D-型含量显著升高,而核心聚集区 D-型含量相对降低,从手性结构层面为理解 AD 蛋白错误折叠与异常聚集提供了新证据。
针对 Tau 蛋白,南开李功玉团队鉴定出19种以上手性异构变体,突破国际同行主要依赖靶向策略、仅能解析单一位点异构化的研究局限(Ryan Julian, J. Proteome Res.2022)。统计结果表明,南开李功玉团队建立的非靶向规模化手性蛋白组学流程将蛋白手性异构变体的年度鉴定数量提升高达2 个数量级(图3A),推动此方向由“单点发现”迈向“系统鉴定”,实现了此领域研究范式的重要跃升。此外,关键位点修饰比例在与国际同行对比分析中高度一致,也充分证明了本方法体系的可靠性、先进性和国际竞争力。
在生物学应用方面,团队围绕阿尔茨海默病相关蛋白Aβ42等代表性体系,研究了特定位点手性异构化对蛋白构象、金属离子结合、聚集行为及细胞毒性的影响(Chem. Sci. 2023/Sci. Adv. 2026)。结果提示,不同位点和不同类型的手性异构化可能对Aβ42的结构性质和相关生物学效应产生不同影响。进一步研究显示,某些临床相关Aβ42立体异构体之间可能存在相互作用,并对纤维形成过程产生影响。这些结果提示,蛋白手性异构化除作为蛋白老化相关化学变化外,也可能参与蛋白聚集及毒性调控。
在此基础上,南开李功玉团队进一步将手性分辨蛋白质组学从哺乳动物体系拓展至农业科学领域,与水稻分子遗传与育种专家万建民院士团队合作,揭示了 D-氨基酸代谢调控水稻垩白形成的新机制(PNAS 2026)。南开李功玉团队在植物体系中系统开展手性分辨蛋白质组学分析,证实水稻胚乳中存在异构化蛋白,并发现 D-氨基酸转氨酶突变可显著改变蛋白异构化水平,导致淀粉和贮藏蛋白合成相关关键酶构象异常,进而诱发内质网胁迫并促进籽粒垩白形成。此研究将手性蛋白组学技术成功用于作物重要性状机制解析,有效拓展了此技术体系的应用边界,也从生物学效应层面反向验证了所建方法的准确性与普适性。
总体来看,李功玉团队围绕蛋白手性变体这一方向,在方法学构建、蛋白质组尺度识别和疾病相关机制探索等方面形成了较为系统的研究工作,推动了相关研究从个案分析向系统研究拓展,也为进一步理解衰老和神经退行性疾病中的蛋白稳态变化提供了新的研究视角。未来,随着分析方法、验证体系和样本范围的进一步完善,这一方向有望在机制研究和标志物发现中发挥更大作用。




