来源:ACS期刊资讯
英文原题:Mapping the Functional Architecture of Influenza A Virus-Induced Phase Separation through m6A Proximity Labeling
通讯作者:刘书琳,南开大学化学学院
作者:贺中达,王逸凡,黄仁堂,胡宇斯,余聪,成垚,王志刚,Don C. Lamb,庞代文
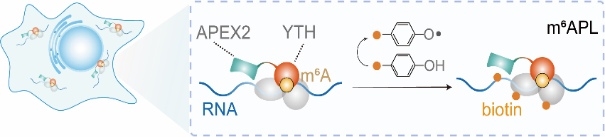
图1.m6APL技术设计原理简图
背景介绍
生物分子凝聚体在细胞功能调控和病毒复制中扮演关键角色。液-液相分离是驱动此类无膜细胞器组装的重要机制,而RNA的N6-甲基腺苷(m6A)修饰在调控RNA代谢和相分离过程中起重要作用。然而,病毒如何利用宿主的m6A修饰系统来构建功能性的相分离“病毒工厂”,仍是未解之谜。传统方法如m6A-RIP、m6A-CLIP等依赖细胞裂解,无法原位感知m6A修饰的RNA及其互作蛋白的空间分布模式,且极易丢失瞬态及微弱的相互作用信息。
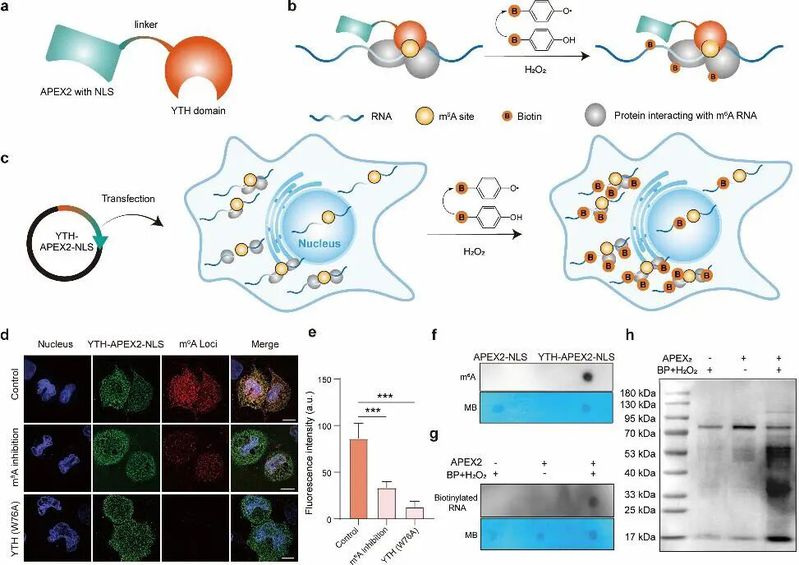
图2.m6APL技术的开发与验证
文章亮点
近日,南开大学刘书琳团队在ACS Nano上发表研究,报道了一种全新的m6A邻近标记技术(m6APL),实现了对m6A修饰转录物的原位亚细胞定位和纳米尺度蛋白质相互作用网络的高精度映射。将此技术应用于流感病毒感染研究中,发现甲型流感病毒(IAV)感染会触发细胞质中相分离包涵体(IBs)的组装,这些凝聚体富含m6A修饰,并作为高效的病毒复制中心。
该技术利用YTH-APEX2融合蛋白在活细胞内对m6A位点及其邻近分子进行特异性生物素标记(图1),从而能够在原位对m6A进行空间成像(m6APL-Img)、对m6A修饰的RNA进行转录组测序(m6APL-Seq),并系统鉴定与m6A RNA相互作用的蛋白质(m6APL-MS)。研究人员设计了一种双功能融合蛋白,将m6A阅读器YTH结构域与工程化过氧化物酶APEX2通过柔性连接子连接,添加了核定位序列。该蛋白能特异性结合细胞内的m6A修饰位点,并在其附近催化生物素-酚生成活性自由基,从而特异性可视化细胞内的m6A位点,并有效生物素化m6A修饰的RNA和与m6A位点相互作用的蛋白质(图2)。这些结果共同证明了m6APL技术的高特异性和可靠性,为后续研究奠定了基础。
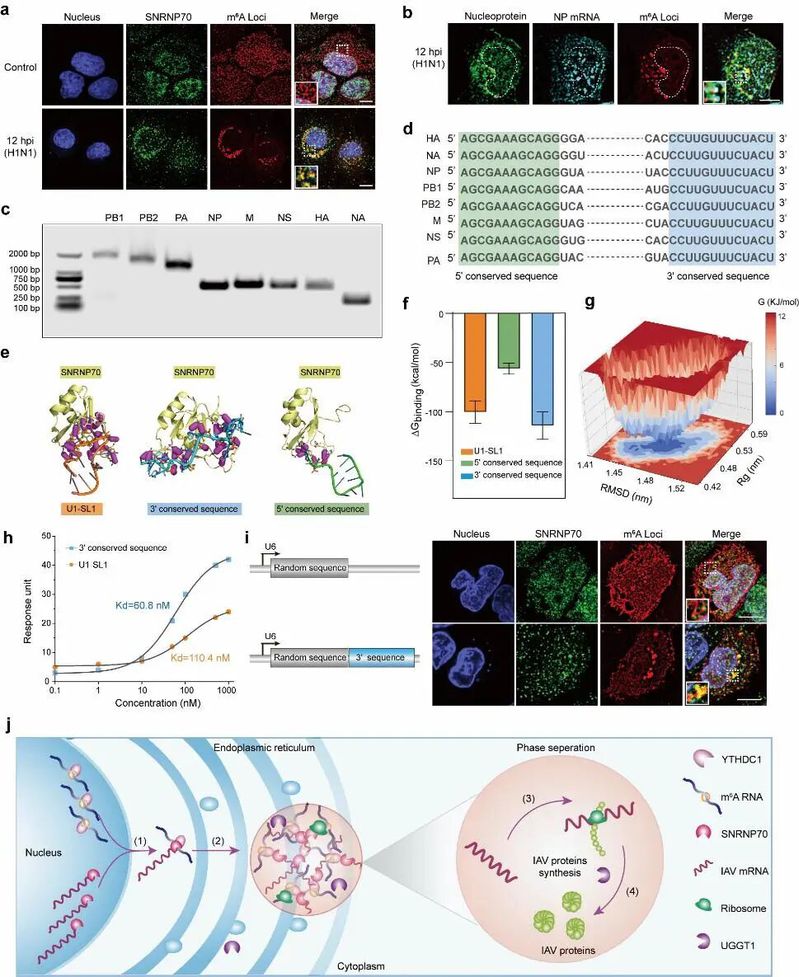
图3. m6APL揭示甲型流感病毒感染诱导形成m6A富集的相分离凝聚体机制
进一步地,将此技术应用于IAV感染的细胞,取得了关键发现。如图3所示,病毒感染后,在宿主细胞质中形成了富含m6A修饰RNA和病毒蛋白的相分离凝聚体。组学分析揭示病毒感染通过上调宿主核糖体相关mRNA的m6A修饰,劫持宿主翻译机制以支持自身mRNA的成熟、转运及蛋白的正确折叠与高效合成。随后的研究表明,宿主剪接体关键蛋白SNRNP70是连接病毒mRNA与宿主相分离机器的关键桥梁,SNRNP70与甲型流感病毒mRNA的3‘保守末端序列具有强结合力,这种强相互作用促使SNRNP70伴随病毒mRNA一同进入细胞质,并在内质网区域通过与m6A阅读蛋白YTHDC1等因子的互作,共同驱动了富含病毒组分和宿主因子的液-液相分离凝聚体的组装。该研究阐明了m6A在核糖体相关mRNA上的上调,以及UGGT1和SNRNP70蛋白质在凝聚体中的富集,共同将IBs重编程为病毒蛋白合成的工厂的机制,确立了m6A介导的相互作用是调控病毒-宿主区室形成和功能的关键。
总结/展望
该研究开发的m6APL技术平台为在纳米尺度、多模态解析表观转录组调控网络提供了通用且强大的工具。通过应用m6APL,研究阐明了甲型流感病毒通过劫持宿主m6A修饰系统和SNRNP70蛋白,驱动功能性相分离凝聚体组装的机制。该凝聚体作为一个高效的“病毒蛋白合成工厂”,其形成依赖于m6A修饰的上调和宿主因子的协同富集。这不仅深化了对病毒-宿主相互作用的理解,也为未来开发靶向病毒相分离过程的广谱抗病毒策略提供了新的理论依据和潜在靶点。
相关论文发表在期刊ACS Nano上,南开大学博士研究生贺中达为文章第一作者,刘书琳教授为通讯作者。




